Striking images capture an antibiotic slaying bacteria in real time
Изучение механизмов действия антибиотиков является одной из наиболее важных задач современной микробиологии и фармакологии. Недавние инновационные исследования позволили не только понять, как антибиотики борются с вредоносными бактериями, но и зафиксировать этот процесс в режиме реального времени с исключительной точностью. Эти открытия открывают новые горизонты в разработке более эффективных средств борьбы с антибиотикорезистентными штаммами и спасают миллионы жизней по всему миру.
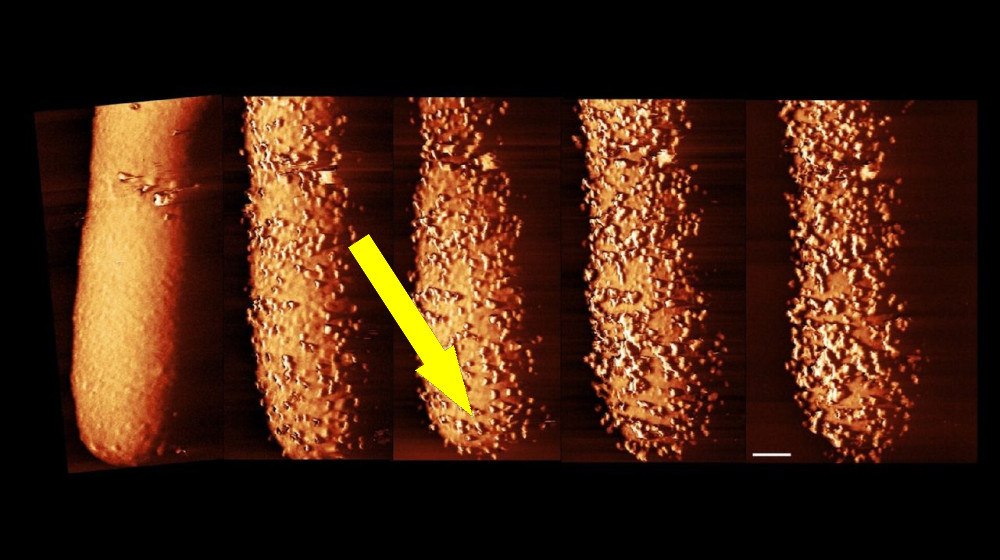
Тонкая борьба: что происходит на поверхности бактерии
Группа ученых из Университетского колледжа Лондона (UCL) использовала новейшие методы микроскопии для наблюдения за процессом уничтожения бактерий на молекулярном уровне. В частности, использовалась технология атомно-силовой микроскопии, которая позволяет получить высокоточные изображения поверхности микроорганизмов и фиксировать динамические изменения в кратчайшие сроки.
В центре внимания оказалась группа антибиотиков, известных как полимиксины, которые применяются для борьбы с стрессоустойчивыми штаммами бактерий-Gram-negative. Эти бактерии характеризуются наличием двух мембранных слоев: внутренней и внешней, причем внешняя мембрана служит мощной защитной бронёй. В числе опасных представителей — Escherichia coli, Salmonella и Shigella, вызывающие различного рода инфекции, в том числе диарею и дизентерию.
Наука в движении: как полимиксины побеждают бактерии
Исследователи зафиксировали, что при контакте с полимиксинами на поверхности бактерии начинают возникать бугорки и выпуклости. Этот процесс схож с тем, как царапина вызывает вздутие кожи — микроорганизмы реагируют на агрессию, пытаясь защититься. В течение нескольких секунд наружная мембрана покрывается множеством таких выступов, постепенно разрушаясь и теряя свою целостность.
“Это было невероятно — видеть, как антибиотик влияет на клеточную поверхность бактерии прямо в реальном времени”, — рассказывает соавтор исследования Каролина Борелли, аспирантка, изучающая биофизику и микробиологию в UCL.
В результате повреждения мембраны бактерия теряет свою защитную оболочку, что позволяет антибиотикам проникнуть внутрь клетки и начать активное уничтожение. Такой механизм разрушения подчеркивает важность понимания микроскопических процессов, что в будущем поможет создавать новые препараты, более эффективно преодолевающие бактериальные защиты.
Технология и методы: как увидели невидимое
Ключевым инструментом исследования стала атомно-силовая микроскопия, которая позволяет «рисовать» поверхность бактерии, передавая точное трёхмерное изображение в реальном времени и с молекулярной точностью. Этот метод отличается от традиционных, потому что он фиксирует не только статическое изображение, а динамику изменений, происходящих при взаимодействии антибиотика с микробной клеткой.
Используя этот подход, ученые обнаружили, что в ответ на воздействие полимиксинов бактерия активирует процесс образования новых "кирпичиков" — белков и молекул, необходимые для восстановления поврежденных участков мембраны. Однако, если повреждения слишком велики или процесс происходит слишком быстро, бактерия не успевает восстановить свою защиту, и она гибнет.
Роль грам-отрицательных бактерий и способы их защиты
Грам-отрицательные бактерии отличаются наличием двойных мембран, что усложняет задачу для антибиотиков, поскольку внешняя мембрана действует как своего рода барьер, отталкивающий большинство лекарственных веществ. Именно поэтому полимиксины, повреждая именно внешнюю мембрану, представляют собой ценный инструмент в борьбе с такими микроорганизмами.
- Полимиксины взаимодействуют с липидами внешней мембраны, вызывая ее дисфункцию;
- После повреждения мембраны бактерия теряет способность удерживать внутренние компоненты внутри клетки;
- Это ведет к быстрому разрушению микроорганизма и гибели бактерии.
Ограничения и перспективы использования
Важно отметить, что полимиксины активны только по отношению к активно растущим бактериям, поскольку их механизмы атаки требуют наличия живых и делящихся клеток. Бактерии, перешедшие в состояние спячки или покоя, обладают способностью избегать воздействия антибиотиков, что создает дополнительные сложности в лечении инфекционных заболеваний.
Учёные предполагают, что следующая задача — это найти способ комбинировать полимиксины с препаратами, стимулирующими активность бактерий, чтобы «пробудить» спящие клетки и обеспечить их уничтожение. Такой подход может значительно повысить эффективность терапии и снизить риск развития резистентных штаммов.
Будущее антибактериальной терапии
Новые результаты не только проливают свет на молекулярный механизм действия полимиксинов, но и позволяют задуматься о разработке более точных и эффективных средств борьбы с устойчивыми к антибиотикам бактериями. Современные инженерные решения и возможности молекулярной микроскопии уже позволяют ученым моделировать и тестировать новые препараты на уровне живых микроорганизмов, не выходя за рамки лаборатории.
Наука движется к тому, чтобы создавать антибиотики, способные повреждать бактериальные мембраны быстрее, точнее и безопаснее, минимизируя побочные эффекты для человека. В условиях роста числа резистентных штаммов и исчезновения новых антибиотиков на фармацевтическом рынке такие исследования крайне важны для будущего медицины.
Заключение
Фиксация процесса разрушения бактерий в реальном времени — это прорыв, который открывает новые возможности для разработки лекарств. Перед учеными стоит задача не только понять механизмы, но и научиться управлять ими, чтобы преодолеть сопротивление бактерий и спасти миллионы жизней. Время показало, что только наука и инновации смогут противостоять эволюции микроорганизмов и сделать наш мир безопаснее.